
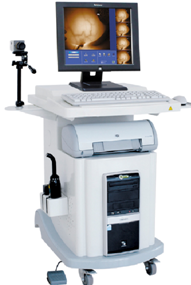
红外乳腺检查仪
医疗器产品主册标准的审查是产品主要技术性能指标审查中最重要的环节之一。
红外乳腺检查仪主要技术性能指标可以分解为技术性能要求和安全要求两部分。其中有些技术性能要求和安全要求又是相关联的。
标准中规定的要求部分是否齐全,可以通过对是否具有以下主要内容进行审评:
1.医疗器械注册红外乳腺检查仪的安全要求
(1)安全要求应符合GB 9706.1-2007标准规定。若为医用电气系统,或使用符合其它电气安全标准要求的零组件,则还应符合GB 9706.15-2008的要求。
2.医疗器械注册红外乳腺检查仪的环境试验要求
设备的环境试验应按GB/ T14710-2009的规定,明确所属气候环境分组和机械环境分组,并在注册产品标准、使用说明书中说明。
设备还应按GB/ T14710-2009中表A1的规定确定环境试验要求和检验项目。
对于含有信息技术产品零组件的设备来说,由于探头、计算机、显示器的工作环境温度、贮存温度往往不一致,因此组成整机后设备的工作环境温度、贮存温度应按企业在注册产品标准中规定的环境条件进行限制,以保证设备的可靠运行。
3.医疗器械注册红外乳腺检查仪的整机性能指标
探头有效光谱波长范围0.8μm~1.5μm;
探头光功率输出可调,最大输出不小于0.2W但不超过1W;
系统图像分辨率不小于400TVL。
对设备主机和与之配套的每一个探头(含选配探头)必须给出下列参数(须在注册产品标准的基本技术参数中列出):
探头发射光的光谱波长范围(单位μm);
探头光输出的峰值波长(单位μm);
本文来源于:深圳鸿远医疗器械咨询
探头的最大光功率输出值及范围(单位mW);
探头的通光孔径(单位mm)。
对于与设备主机配套的摄像机必须明确:
摄像机光谱响应曲线相关参数。
上述参数指标原则上应符合YY 0324-2008标准的要求。
此外,对于含有计算机软件的检查仪,还应在注册产品标准的基本技术参数中明确软件正常运行所需的计算机硬件配置和系统软件条件。
4.医疗器械注册红外乳腺检查仪的正常工作条件(包括环境温度、相对湿度、大气压力、电源等)。
5.医疗器械注册红外乳腺检查仪的外观和结构要求:由制造商在注册产品标准中明确,如:
(1)仪器表面应光洁、色泽均匀、无伤斑、划痕、裂纹等缺陷,面板上文字和标志应清晰;
(2)控制和调节机构应灵活、可靠,紧固部位应无松动。
6.医疗器械注册红外乳腺检查仪的探头的生物相容性要求:预期与体表进行一时接触(〈24h),按GB/ T16886.1-2001给出的指导原则进行评估,提供相关评估资料证明细胞毒性试验、过敏试验和皮内刺激试验符合相关标准要求,必要时需要提供有资质检测单位出具的生物相容性试验报告。
7.医疗器械注册红外乳腺检查仪的使用功能要求(包括软件功能):例如:探头工作波长选择、探头识别、电影回放、增益调节范围、图像放大倍率、焦点选择、灰阶分级、工作模式选择、边缘增强级数选择、动态范围级数、字符和标志显示、测量和计算、管理功能、图像处理或打印功能等,但必须明确产品软件不涉及图像分析功能。
深圳鸿远医疗器械咨询有限公司是一家医疗器械领域值得信赖,务实高效,创新权威的医疗器咨询服务机构,为医疗器械生产及销售企业提供专业的医疗器械技术咨询服务机构。专注于医疗器械注册代理,医疗器械注册咨询,医疗器械经营许可证办理,医疗器械生产许可证办理,进口医疗器械注册医疗器械备案,计量生产许可证办理, FDA注册,ISO13485认证及CE认证标,临床试验,医疗器械分类,洁净室设计指导,医疗器械质量管理体系认证及体系建立与过程确认文件建立(ISO9001, ISO13485, GMP, CE,QSR820,CMDCAS);注册,出口证,自由销售证办理,产品检测,临床试验及免临床资料编写,产品技术要求制订,技术文件编写辅导等.
8.医疗器械产品注册红外乳腺检查仪的电磁兼容性要求:应符合YY 0505-2005等相关标准要求。

 在线客服
在线客服